이중 표적 CAR-T 치료의 고형암에 대한 연구
페이지 정보
작성자 HK HIS 작성일21-10-17 20:49 조회1,792회 댓글0건관련링크
본문
이중 표적 CAR-T 세포 치료는 고형 종양을 보다 효과적으로 치료할 것으로 예상됩니다.
2021년 9월 29일 새로운 연구에서 채플힐에 있는 노스캐롤라이나 대학의 연구원들은 유전자 변형 T세포를 사용하여 종양을 공격하는 새로운 방법을 발견했습니다. 암세포에 대한 두 가지 항원은 인간 신경모세포종 조직이 이식된 실험에서 매우 효과적이었습니다. 이 이중 표적화는 종양의 재성장을 제한하고 신경모세포종 세포가 이러한 공격적인 T 세포를 회피하는 것을 방지합니다.

관련 연구 결과는 2021년 9월 네이처 암학회(Nature Cancer)에 게재되었습니다. 신경모세포종은 주로 6세 미만의 어린이에게 발생하는 미성숙한 신경 세포의 암입니다. 이 종양 은 일반적으로 부신의 상단에서 발견되지만 복부, 가슴, 목, 골반 및 뼈에서도 발생할 수 있습니다. 미국에서는 매년 약 500~1,000명의 신경모세포종 환자가 발견되고 있습니다.
논문의 공동 제1저자이자 공동 교신 저자인 Dr. Hongwei Du는 “종양 세포의 특징은 이중 표적 T 세포를 설계하여 종양이 면역계의 탐지를 회피하는 것을 방지하는 능력을 최대화합니다. 또한 이러한 유전자 변형 T 세포도 중요한 신호를 받을 수 있습니다. 고형 종양을 극복하기 위한 특정 유형의 면역 요법에서 발견됩니다. 다양한 종양 치료에 항상 많은 도전이 있었습니다. ” 연구원들은 CAR-T 세포 면역 요법을 사용했는데, 이는 환자의 면역 체계에서 T 세포를 수집하고 실험실에서 유전적으로 재생하여 암 세포가 환자의 신체에 재 주입될 때 표적에 암세포의 표면을 식별하는 것을 포함합니다. 구체적으로, 저자는 두 가지 주요 공동 자극 분자인 CD28 및 4-1BB와 함께 종양 세포에서 발현되는 두 가지 항원을 확인 했습니다 . CD28은 초기 활성화 후 T 세포의 표면에 발현되는 단백질이며, 4-1BB는 T 세포의 생존과 기억 형성에 관여합니다. 임상 연구에서 CD28과 4-1BB는 단독으로 사용할 때 혈액 매개 암 환자에게 동등하게 효과적입니다. 그러나 CD28과 4-1BB 공동 자극의 조합은 고형 종양에 중요한 것으로 보입니다. 연구 작업을 통해 이 두 신호를 효과적으로 전송하는 방법을 개발하게 되었습니다.
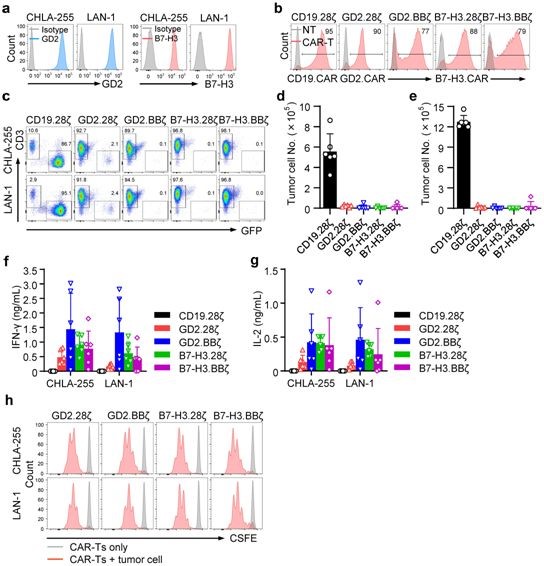
GD2-특이적 CAR-T 세포 및 B7-H3-특이적 CAR-T 세포는 시험관내 신경모세포종을 표적화합니다. Fig. 2는 Nature Cancer, 2021, doi:10.1038/s43018-021-00244-2에 있는 자료입니다. 저자들은 먼저 실험실에서 신경모세포종 세포를 관찰하여 면역 세포의 복합 공격에 어떻게 반응하는지 확인했습니다. 실험실 연구의 긍정적인 결과를 고려하여 그들은 CD28 및 4-1BB를 발현하도록 유전자 변형된 T 세포와의 공동 자극에 어떻게 반응하는지 확인하기 위해 신경모세포종이 이식된 실험쥐를 관찰했습니다. 실제로, 이러한 공동자극 T 세포는 신경모세포종이 많은 실험에서 암을 줄이데 효과를 입증했습니다. 채플힐 의과대학의 노스캐롤라이나 대학교 미생물학 및 면역학 과 교수이자 이 논문의 공동 교신저자 인 (Gianpietro Dotti) 박사 는 다음 과 같이 말했습니다. 이번연구를 통해 우리는 신속하게 종양을 제거할 수 있는 CAR-T를 생성하고, 계속해서 종양 성장을 조절합니다. 종양세포 또한 재발을 예방할 수 있습니다 ." 이 치료법이 실험에서 처럼 인간에게도 유망하다면 종양 세포에서 발현되는 3개, 4개 또는 그 이상의 항원을 표적으로 하는 것이 더 효과적일 수 있다고 저자들은 말합니다 . 과도한 자극은 부작용을 기하급수적으로 증가시킬 수 있기 때문에 조심스럽게 진행할 것입니다. 이러한 상황을 처리하기 위해 이 저자들은 Dotti, Dr. Barbara Savoldo, University of North Carolina at Chapel Hill의 Reinberger Immunotherapy Program 기술을 사용하여 자 극 수준을 조절할 수 있다고 하였습니다.
참고문헌
Koichi Hirabayashi et al. Dual-targeting CAR-T cells with optimal co-stimulation and metabolic fitness enhance antitumor activity and prevent escape in solid tumors. Nature Cancer, 2021, doi:10.1038/s43018-021-00244-2.
Tiffany R. King-Peoples et al. Splitting signals drives CARs further. Nature Cancer, 2021, doi:10.1038/s43018-021-00257-x.