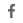표적 항암 임상
관련링크
본문
쿠바백신(CIMAvax)
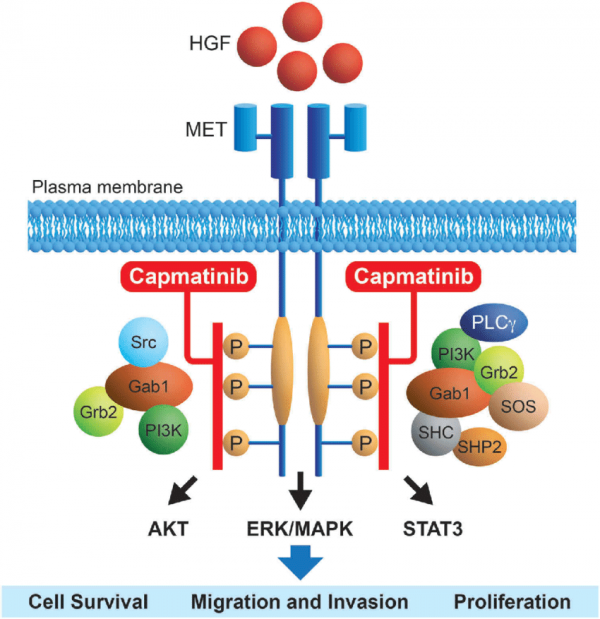
쿠바백신(CIMAvax)은 비소세포 폐암 3기 혹은 4기 (뇌전이 제외) 환자를 대상으로 EGFR(HER-1) 유전자 변이를 표적으로 하여, 쿠바의 분자 면역 센터(Cuban molecular immunology Center)에서 개발한 백신입니다. EGFR(Epidermal growth factor receptor)은 건강한 세포와 폐암 세포에서 발견되는 단백질로써, 폐암 환자의 약 15%에서 EGFR 돌연 변이가 발생하는 것으로 보고되고 있습니다. 1990년 암 연구자들은 EGFR이 폐암 발병을 촉진 할 수 있다고 믿었기 때문에 Abitus, Trocaine, lressa, Lapatinib와 같은 EGFR 단백질을 표적으로 하는 약물을 개발 했습니다. 이러한 약물은 EGFR이 특정 돌연변이를 생성 할 때만 작동합니다. 표피 성장인자(EGF, Epidermal growth factor)는 EGFR을 자극하여 세포 분열을 촉진하게 되는 정상적 세포분열 과정을 거치는데, EGFR에 유전자 변형이 발생하게 되면, EGF의 촉진 없이도 EGFR은 세포분열을 촉진시키는 역할을 하게 되는 것입니다. CIMAvax는 면역세포를 자극하여 EGF에 대한 항체 작용을 하도록 하는 백신으로 EGF의 활동을 저해하여, 암세를 사멸하도록 유도하는 것 입니다. 이 백신은 표적 약물 대비 심각한 부작용을 일으키지 않고, 주사 부위에 통증, 열, 구토 및 두통 정도의 가벼운 부작용을 일으키게 됩니다.
관련자료: https://www.roswellpark.org/cimavax
임상결과 1
CIMAvax는 비소세포암(NSCLC) 환자 5000명을 대상으로 수행한 임상실험에서 안전하고 효과적인것으로 입증되었습니다. 3상 임상 시험에서는 백신 접종 환자의 경우, 비 대상 환자 대비 2개월 이상의 생존 기간이 증가한 것으로 나타났고, 5년 생존율은 비 접종 환자의 경우 7.9%를 보였음에 비해 14.4%로 두배 가까이 높은 결과를 보였습니다.
임상결과 2
첫번째 시험에 71명의 환자가 선발되었으며, 실험 결과는 2007년 12월 의학저널 Cancer Biology &Therapy에 발표되었습니다. 환자가 받은 화학요법은 대부분 4~6주기 동안 카보플라틴과 빈블라스틴 이었고, 백신 투약에 따른 실험 결과 평균 생존율, 1년이상 생존율을 모두 증가 시킨 것으로 나타났습니다.
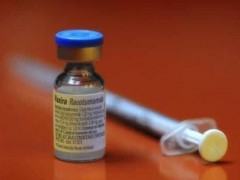
캡마티닙(INC280)
캡마티닙(Capmatinib, INC280)은 노바티스에서 개발한 MET억제제이며, 2020년 현재 FDA에 의해 우선심사 대상으로 선정되었습니다. MET 돌연변이는 전이성 비소세포폐암에서 약 3~4%를 차지하는 드문 유형으로 알려져 있고, 예후가 나쁘게 진행됩니다. 현재까지 MET 돌연변이에 폐암에 대한 공식적으로 승인된 표적 약물은 없습니다.
임상결과 1
1세대 표적항암제 게피티닙과 병용된 캡마티닙(INC280)의 1상/2상 연구에서 MET 증폭환자에서 EGFR 돌연변이 및 MET장애를 갖는 비소세포암(NSCLC)에 대한 유망한 치료법인것으로 나타났습니다.
임상결과 2
2018년 11월 8일 기준 비소세포암 MET Δex14 돌연변이 97명(코호트 4: 69명; 코호트 5b: 28명)에 대해 평가 하였습니다. 독립 판정단(BIRC, Blinded Independent Review Committee)에 의한 ORR (95 % CI)은 코호트 4에서 39.1% (27.6-51.6)이고, 코호트 5b에서 71.4%(51.3-86.8)였습니다. 여전히 미성숙 한 분석을 보이는 이 시점에 , 내구성에 대한 데이터는 믿을 만 합니다. BIRC에 의한 중간 DOR (95% CI)은 각각 코호트 4 및 5b에 대해 9.72(4.27-11.14) 및 8.41(5.55-NE)를 보였고, PFS (95 % CI)는 코호트 4 및 5b에 대해 각각 5.42(4.17-6.97) 및 9.13 (5.52-13.86) 를 보였습니다. 모든 코호트 (n = 315)에서 가장 흔한 역효과 (≥ 25 % 모든 등급)는 말초 부종(49.2 %), 구역질(43.2 %) 및 구토(28.3 %)였습니다.
관련자료: https://ascopubs.org/doi/abs/10.1200/JCO.2019.37.15_suppl.9004
AMG510
AMG510은 암젠(Amgen)에서 개발한 KRAS G12C 돌연변이가 있는 환자를 대상으로 하는 경구형 표적 항암제입니다. 이 유전자 변이는 폐암에 나타나는 다른 돌연변이(예: ALK, BRAF 및 EGFR)보다 더 많은 빈도로 나타나는 것으로 보고되고 있어, 이 치료제는 폐암 환자에게 좋은 소식입니다. 이 KRAS G12C 돌연변이는 일반적으로 폐암 환자의 약 13%, 결장/직장암 및 충수암 환자의 3% 및 다른 고형 종양환자의 1~3%에서 발생합니다. 그리고 90%의 췌장암, 30~40%의 결장암 및 30% 이상의 폐선암종에서 나타난다고 알려져 있습니다. 2019년 ASCO컨퍼런스에서 AMG510은 성공적으로 1단계 연구 결과를 발표 했습니다.
임상결과 1
고형종양에서 국소 진행성 또는 전이성 KRAS G12C 돌연변이를 가진 성인 환자에서 처음 수행된 다기관 공개 1상 임상 연구 입니다. 총 35명 환자(비소세포 폐암 14명, 결장/직장암 19명, 충수암 2명)가 시험에 등록했습니다. 35명 환자 각각 180mg, 369mg, 720mg 및 960mg의 용량으로 AMG510을 투약하도록 무작위로 배정 되었고, 시험 결과 비소세포암 10명 중 5명이 부분적으로 완화 되고, 4명이 안정적이고 , 1명만 질병 진행을 보였으며, ORR은 50%, 질병 관리율은 90%였습니다. 부분 완화가 있는 5명의 환자는 여전히 약물을 복용하고 있습니다.