KRAS変異薬trimetinib
페이지 정보
作成者 HK HIS 作成日19-09-16 18:20 照会371回 コメント0回관련링크
본문
KRAS遺伝子の突然変異は、現在、世界で最も困難な遺伝的変異です。 TrimetinibはMAPK経路に影響を及ぼし、主にMEKタンパク質の作用を介して細胞増殖を抑制するMEK1 / 2阻害剤です。 MEKは、RASとRAFのダウンストリーム信号伝達タンパク質であるので、trimetinibはまた、RASまたはRAF変異がある癌に有効であることができます。 FDAは共同、ネパールBRAFV600E突然変異の治療のための遺伝子の突然変異のBRAFV600EまたはV600K切除不能または転移性悪性黒色腫と転移性非小細胞肺がん(NSCLC)とシアリスの治療に承認されました。
trametinibについて
TrimetinibはMAPK経路に影響を及ぼし、主にMEKタンパク質の作用を介して細胞増殖を抑制するMEK1 / 2阻害剤です。 MEKは、RASとRAFのダウンストリーム信号伝達タンパク質であるので、trimetinibはまた、RASまたはRAF変異がある癌に有効であることができます。
米国医薬品名:Mekinist
サプライヤー:Novartis / Glaxo
次は、trimetinibの分子式です:
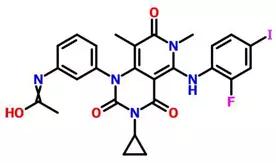
FDAは、trimetinib 2017年6月22日に承認されており、BRAF V600E突然変異陽性転移性非小細胞肺がん(NSCLC)患者にダラフィニ(darafini)と併用投与しました。これはBRAF V600E突然変異陽性転移性非小細胞肺がん患者の治療のために特別に承認された最初のFDAです。
2014年1月10日にBRAF V600E突然変異陽性メラノーマ患者の治療でダラペニー(darafene)と併用されたトラマチニプ(trametinib)は切除されたり転移することができない良性です。
2013年5月29日BRAF V600EまたはV600K突然変異で切除不可能または転移性メラノーマ患者の治療を対象としています。
trimetinibの臨床効果は何ですか?
1. BRF113928(NCT01336634)
2017年6月22日、FDAはBRAF V600E突然変異陽性転移性非小細胞肺がん(NSCLC)患者にtrimetinibとdarafiniを承認した。承認は2相臨床試験BRF113928のデータに基づいています。
実験的設計:
93患者は、ツリーのメタジディンイエローティーニブ(口頭回2mg)を、初期治療36例、57例は化学療法を受けた結合ダラフェニックス(口頭回150㎎)を受けた。
実験結果:
治療後、新たに診断された患者群の全体反応率は61%に達した化学療法を受けた患者の全体的な奏効率は63%であった緩和期間の中央値は12.6ヶ月であった。
人間の健康を脅かす一般的な悪性腫瘍で、世界で毎年約1千8百万人の肺癌と診断され、そのうちの80%以上が非小細胞肺癌では、すべての非小細胞肺がん患者のうち1〜3%の患者は、BRAF V600変異がています。また、過去にこのようなタイプの患者グループの主な治療法は、化学療法であり、他のいくつかのオプションがありました! dabrafenibとtrametinibの併用療法が出現して、欧州委員会と米国FDAの承認を受けた後に肺がんの治療の分野で重要なマイルストーンとなりました!
副作用:
発熱、下痢、吐き気、嘔吐、疲労、発疹、食欲不振、浮腫、咳などの症状、重篤な副作用無し、安全性制御が可能。
2 メラノーマI / II研究
2014年に米国FDAは、手術不可能か転移性メラノーマのBRAF V600EまたはV600K突然変異治療にMEK inhibitor trimetinibとBRAF inhibitor dalafinibの併用を承認した。承認は公開I / IIの調査に基づいています。
実験的設計:
進行メラノーマの総162人の患者を登録してtrimetinibとdalafiniをマージ投与した。
研究結果:
dalafini単独療法と比較すると、trimetinibとdalafiniの組み合わせは、全体の奏効率(ORR)を効果的に増加させることができます。 76%の患者で腫瘍が縮小されたり消える平均時間は10.5ヶ月であった。対照的に、研究者は、ダラペニーブ単独治療を受けた患者の54%が、平均腫瘍収縮があったり、5.6ヶ月の消失を発見した。
副作用:
発熱、悪寒、倦怠感、発疹、吐き気、嘔吐、下痢、腹痛、手と足の腫れ、咳、頭痛、関節痛、夜汗、食欲減退、便秘、および筋肉痛。深刻な副作用には、出血、血栓、心不全、皮膚、目の問題は、腎臓の損傷などがあります。
FDAは妊娠可能年齢の年齢の女性であるtrimetinibとdalafiniは乳児先天性奇形児を勧告し、trimetinibとdalafiniを使用した治療は、不妊を引き起こすことが指摘されなければならないと強調した。
3メラノーマの無作為二重盲検研究
2013年5月に、FDAはBRAF V600EまたはV600K突然変異で切除不可能または転移性メラノーマを治療するためにトラマチニプ(MEKINIST、GlaxoSmithKline)を承認した。
実験的設計:
≤1化学療法を受けた322人の患者のためにマニホールド、国際公開、無作為二重盲検研究
研究結果:
4.8ヶ月PFS比較Trametinib療法グループました:8%:1.5ヶ月(P <0.0001)、客観的な反応率は22%であった。推奨容量は次のとおりです病気の進行や我慢でき毒性までTrametinib 2mgを含むのQD(前や2時間食事の後1時間)。一般的な副作用としては、発疹、下痢、およびリンパ浮腫があります。 BRAF V600E突然変異を運ぶの治療のための単一のエージェントが、手術または切除不能または転移性メラノーマのメラノーマ成人患者をV600KにMekinist(trametinibは)するMEK阻害剤、経口用タブレットをした。
副作用:
発疹、下痢、およびリンパ浮腫。
トラマチニプを服用している患者に表示される深刻な副作用としては、心筋症、網膜色素上皮剥離、網膜静脈閉鎖、てんかん肺疾患と重度の皮膚毒性などがあります。
この薬をインポートする方法?
MEKINISTで治療する前に、腫瘍サンプルからBRAF V600EとV600K突然変異があることを確認しました。
MEKINISTに推奨される容量療法は、単一の薬剤として1日2回経口で1日2回経口で一日150mgを服用しているdabrafenibです。 MEKINISTは食事前少なくとも1時間以上食事の後、少なくとも2時間以上服用してください。
用法形態と規格
精製:0.5 mg、1 mg、および2 mg。
使用上の注意すべき点は何ですか?
新しい原発性悪性腫瘍、皮膚および非皮膚:MEKINISTとdabrafenib併用時に発生することがあります。治療前、治療後、併用療法終了後、新しい悪性疾患について観察した。
出血:大出血の事件は、dabrafenibとMEKINISTを受ける患者で発生する可能性があります。出血性の徴候と症状をモニターしてください。
静脈血栓塞栓症:dabrafenibとMEKINISTを投与される患者の深部静脈血栓症と肺塞栓症が発生する可能性があります。
Cardiomyopathy:LVEFは治療1ヶ月後、2〜3ヶ月ごとに評価された。
眼球毒性:視覚障害の眼科的評価。網膜静脈閉鎖(RVO)の場合には、MEKINISTを完全に終了します
間質性肺疾患(Interstitial lung disease、ILD):MEKINISTは新しい進歩的なものとして説明することができない肺の症状を誘発しません。 MEKINISTは、治療に関連するILDと肺炎に恒久的に終了します。
重度の発熱反応:MEKINISTとdabrafenib併用時に発生することがあります。
重度の皮膚毒性:皮膚毒性と二次感染を監視してください。耐えることができない2年生と3年生と4年生の場合は、MEKINISTを中断しても、3週間以内に薬物治療が改善されていない。
高血糖:既存の糖尿病および高血糖患者の血清グルコース値を監視します。
胚胎児毒性:胎児に害を及ぼす可能性があること、胎児の生殖潜在的な危険がある女性にアドバイスしてください。
一般的な副作用は何ですか?
MEKINISTは一般的な副作用(20%以上)で発疹、下痢、およびリンパ浮腫が含まれています。
最も一般的な副作用(≥20%)と一緒にdabrafenibに隠れメイエルランロティありませは、発熱、悪寒、倦怠感、発疹、吐き気、嘔吐、下痢、腹痛、末梢浮腫、咳、頭痛、関節痛、冷や汗、食欲の損失を含む減少された、便秘および筋肉痛。
MEK紹介:
MEKは、科学者たちの初期の発見されて研究された標的の一つです。 MEK(水戸ゲン活性化プロテインキナーゼ)とMEK2 MEK1に分けることができるしているRAS-RAF-MEK-ERK経路の重要なシグナル伝達分子、細胞増殖、細胞死滅、細胞分化は、側面が重要な役割をする腫瘍。
MEKの臨床試験での行動の複数の高級大腸癌、例えば、口腔MEK阻害剤CI-1040の薬物が対象で、非小細胞肺癌、乳癌や膵臓癌患者の臨床試験段階IIの複数であり、それを見ました。 AZD6244(sterminibとも呼ばれる)は、Q56PとK57N突然変異で腫瘍細胞の増殖を抑制します。
多くの種類のがん発症がMEKに関連しており、MEKの阻害が様々な癌を調節するための手段の一つになったことがわかります。今までは、MEKと目標ネクサバール数テントを含む複数のターゲットに加えて、MEKの特別な一つの抑制があり、Trametinib(Qumeiのプラセボ/ Mekinist)でSelumetinib(AZD6244 / selumetinib)、また、前述したCI-1040がています。
もちろん、MEK阻害剤が使用され、MEK遺伝子の存在が検出されなければならない。
推奨される臨床試験(患者が申請することがあります):
1.再発または兵器IV KRAS変異陽性非小細胞肺がんの治療でもメタセルと結合したトラマチニプ。 (NCT02642042)
この2相試験は、tramETinibとdocetaxelこの兵器がKRAS変異陽性非小細胞肺がんまたは再発したがん患者の治療にどのように貢献するかを調査した。 Trametinibは、細胞の成長に必要ないくつかの酵素をブロックすることによって、腫瘍細胞の成長をブロックします。ドセタキセル(docetaxel)などの化学療法で使用される薬は、腫瘍細胞の成長をさまざまな方法でブロックしたり、細胞を殺すか、分裂を防ぐか、拡散を防止します。 trametinibとdocetaxelの投与は、非小細胞肺がんのためのより良い治療法になることがあります。
実験場所:
1. University of California、Davis総合がんセンター
2.ロサンゼルスがんセンター
患者は、グローバル腫瘍マイクロチャネルパブリックネットワーク番号を懸念することも、臨床試験に参加する医療記録を提出するように指示に従ってください、医療部門は予備の適合性を評価し、可能な限り迅速に連絡をあなたと一緒に、詳しくは400-666-7998に電話してください。
2. BRAF V600E-突然変異(まれ腫瘍)患者からのdalafiniとTrametinibの有効性と安全性(NCT02034110)
この未分化甲状腺癌、胆道癌、消化管間質腫瘍、元の精子細胞非生殖細胞腫瘍、非悪性細菌を含む希少がん患者のための非ランダム、オープンラベル段階II Dabrafenib共同Trametinibのマルチセンター研究である細胞腫瘍、毛細胞白血病、神経膠腫1または2、3または4(上級)、神経膠腫、多発性骨髄腫および小腸癌、BRAF V600Eポジティブ-mutations。この研究では、患者の口腔Trametinib治療珍しいBRAF V600E突然変異総有効率(ORR)とともに経口ダラスフェニックスを決定するために設計されました。被験者は、BRAF V600E突然変異状態を確認するために、新規または凍結された腫瘍組織サンプルを提供する必要があります。組織学は、高度な病気と診断されて、標準の治療法がない被験者のみ登録することができます。被験者は、治療開始前に、研究に含める資格かどうかを決定するために、14日以内に眼科検診(眼科検診、シーム超音波検査)を実施することです。
実験場所:
1. UCLA /ジョンソン総合がんセンター
2. MDアンダーソンがんセンター
3.国立衛生研究所臨床試験センター
4.マサチューセッツ総合病院
5.ブレゲンと女性の病院