肺がん治療のCAR-T治療の方向
페이지 정보
作成者 HK HIS 作成日19-09-16 18:20 照会177回 コメント0回관련링크
본문
ニューヨークがん研究所(CRI Cancer Research Institute)は、グローバル腫瘍免疫治療の発展の傾向に関する調査報告をNature Reviews Drug Discoveryに発表しました。 1年間の調査の結果、腫瘍免疫治療に関するグローバルプログラムの数は67%、ターゲット研究は、50%が増加し、臨床開発プログラムに参加している企業や政府機関は42%に増加した結果を示し、腫瘍免疫治療に多くの研究が集中したことが明らかになりました。2011年ipilimumabが黒色ジョンアム治療に承認されたことが、腫瘍免疫治療の革命的事件で始まり、癌治療のパラダイムを変えました。これまで11種の新しい腫瘍免疫療法が承認され、さまざまながんの治療基準となっています。 2011年ipilimumabが黒色ジョンアム治療に承認されたことが、腫瘍免疫治療の革命的事件で始まり、癌治療のパラダイムを変えました。これまで11種の新しい腫瘍免疫療法が承認され、さまざまながんの治療基準となっています。ニューヨークがん研究所は、65年以上にわたり、がん免疫治療研究をしてきた非営利団体として、2017年の世界の腫瘍免疫治療の現状を伝授調べたところがあります。調査の結果は、次のような事項を話しています。世界腫瘍免疫の開発プログラムは、67%レベルの成長率で急速に増加しており、作用のメカニズムに基づいて、免疫治療薬を6種類に分けることができるとしました。これは標的T細胞免疫調節剤(例えば、PD1またはCTLA4のモノクローナル抗体)、およびその他の免疫調節剤(例えば、TLRまたは干渉小 - アルファ/ベータ受容体1(IFNAR1)の刺激)、腫瘍ワクチン(例えば、( BCG)ワクチン)、細胞療法(例えば、インピーダンス抗原受容体(CRA)またはT細胞受容体(TCR)T細胞療法)、ポリープウイルス(例えば、T-vec)、CD3双方向特異性標的抗体(例えば、blinatumomab )です。 6台タイプの免疫療法の細胞療法113%で最も急速に増加している一方で、ポリープウイルスの研究は、16%にとどまり、成長が遅く確認された。また、セピョ療法は、最も多くの研究が行われている技術がされていて、進行しているプログラムの数は864個で、全体の腫瘍免疫プログラムの25%を占めました。
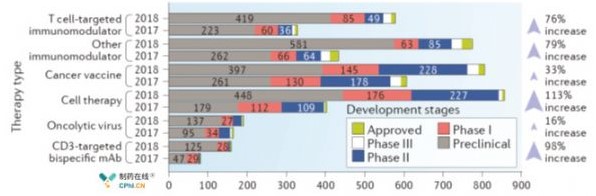
図1の免疫療法プログラムの傾向2018年9月まで
現在、世界の腫瘍免疫治療プログラムでは、417個の標的を研究中です。過去1年の間に免疫治療標的に関する研究が50%増加した。興味深いのは、2017年の研究開発(R&D)の半分は上位23個の標的に集中されたが、2018年には上位48個の標的に集中しました。通常ターゲットつの薬物が承認され、対応する研究開発プロジェクトの数が減少します。例えば、2018年に細胞療法の数が113%増加したにも関わらず、CD19標的抗細胞療法はわずか37%増加した。一方、標的が新しい抗原に加わる薬(オブジェクトの患者の腫瘍の生体情報学的分析に確定された標的)の研究では、1年の間に133%増加しました腫瘍免疫治療標的数の増加は、将来的に、より多くの免疫療法が承認することができるベースになります。注目すべき点は、非特異性腫瘍関連抗原(TAA)薬物の実際の数が減少するということで、これは、領域がより正確な方向に発展している示しています
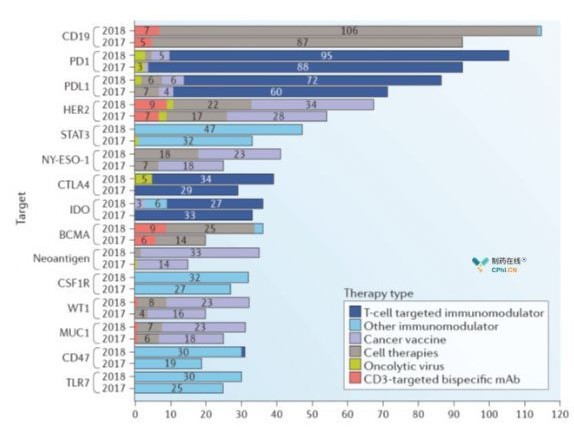
図2免疫治療TOP15標的
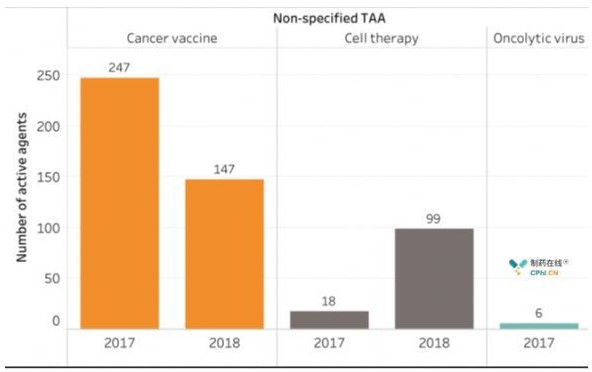
図3非特異性腫瘍関連抗原の項目の傾向
2017年9月461個の組織(バイオ製薬会社)の964個の腫瘍免疫薬が臨床段階に入っており(臨床完了を含む)、1年後に655個の組織が1287個の臨床医薬品開発を進めたのは臨床段階の薬剤の数34%増加した場合と臨床薬物を進めていることを意味します。臨床項目上位15社と比較すると、1年36新薬が20%増えました。さらに重要なのは、Big Pharmaはまだ臨床プログラムの主導的位置を占めており、プログラムすることができ、上位8個をすべてリードしています。 4つの科学研究機関の臨床プログラムは、上位15個に入った中で3つの機関は、中国の深セン市、免疫遺伝子治療の研究301病院第3群医学部第1付属病院で、中国の研究機関が含まれています。
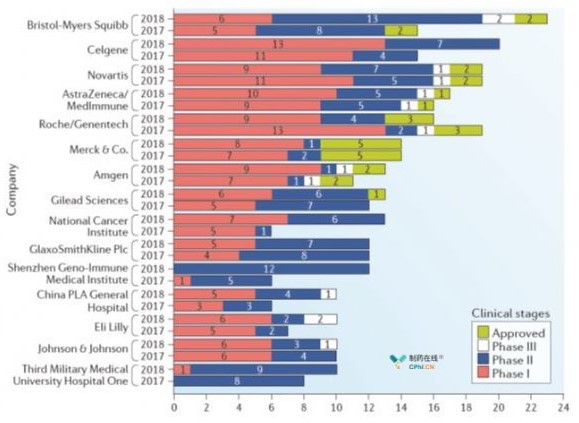
図4 TOP15免疫療法企業や機関
新しい調査分析を介して、1年の間に腫瘍免疫治療のグローバルプログラムの数が67%標的治療50%の薬物の臨床開発が進行中の企業や機関の数が42%増加した。これらの巨大な増加は、腫瘍免疫治療薬の開発のために、私たちの強力な情熱と自信を示します。ニューヨークの研究チームが調査が勤政的に示された理由は、まず、全体の調査(2017年)以来、1年間で10個のアイテムのFDAの承認を受けてCAR-T療法2件PD1とPDL1抗体薬物8件CD3双方向標的特異性抗体が含まれてい。次に、2011年以来、新しい免疫療法は、15種類の癌のタイプの標準的な治療法だけでなく、黒色腫、肺がん、腎臓がんの一般的な治療と免疫療法は、がんの治療の主な研究の支えの一つになりました。 免疫治療の抗PD1とPDL1私は最近の主要な市場である中国に承認されました。まさにNivolumab(製品名:オディーヴォ)とpembrolizumab(商品名:キットホルダー)があります。最後に、多くの臨床研究では、免疫療法は、患者に継続的な生存に助けを与え、がん患者の治癒の希望を実現させたことを証明しました。しかし、まだ潜在的な癌免疫学の問題があります。これに相補的な研究が必要であり、治療率を高める研究が臨床を通じて発展することが予想されます。